DIFFÉRENTS ÉTATS DE L’HYDROGÈNE SOLIDE

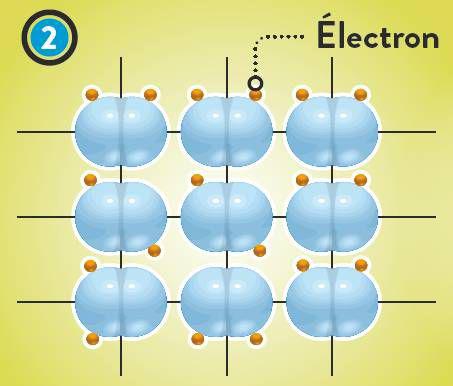
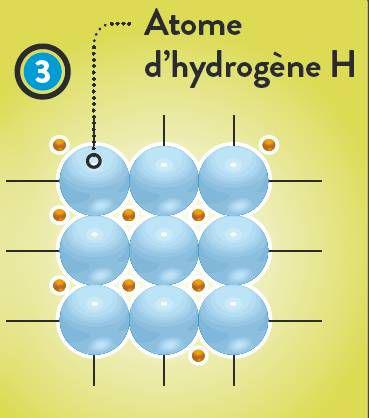
Les chercheurs ont injecté dans leur dispositif du dihydrogène (H) gazeux : chaque molécule de est constituée de 2 atomes d’hydrogène (H). Pour solidifier le gaz, il faut d’abord faire monter la pression… et baisser la température. Que se passe-t-il alors? Dans un premier temps, les atomes d’hydrogène restent en couples et les molécules de H s’organisent de manière régulière au sein de ce que les physiciens nomment « un cristal » . Étrangement, cette structure évolue très peu lorsque la pression augmente. En revanche, au-delà de 425 GPa, les électrons sont expulsés des atomes et peuvent alors circuler librement : c’est l’état «métallique moléculaire» . Hélas, dès que la pression redescend, les électrons rentrent illico au bercail… Mais au-delà de 500 GPa, les chercheurs pensent pouvoir créer une forme «métallique atomique» stable, en brisant les liaisons entre les atomes des molécules : les électrons demeureraient libres même en relâchant la pression .
Vous lisez un aperçu, inscrivez-vous pour lire la suite.
Démarrez vos 30 jours gratuits

